(共6分) 实验室制备少量硅一般采用镁粉还原SiO2的方法,然后用稀盐酸洗涤产品以除去杂质。某同学在进行上述操作时,在制得的产品中加HCl洗涤时突然起火。
(1)请用化学方程式解释:
①稀盐酸洗涤产品可除去哪些主要杂质?
②为什么加HCl洗涤时突然起火?
(2)请设计一个实验来验证你的解释。(不必画出装置图,也不必指出具体化学药品,不要写方程式,只要简明指出方法。)
知识点:综合性实验
1.(共6分) (1) ① 2HCl+MgO![]() H2O+MgCl2
H2O+MgCl2
2HCl+Mg![]() H2↑+MgCl2
H2↑+MgCl2
② SiO2+4Mg![]() Mg2Si
+2MgO
Mg2Si
+2MgO
Mg2Si+4HCl![]() SiH4+2MgCl2
SiH4+2MgCl2
SiH4+2O2![]() SiO2+2H2O
SiO2+2H2O
(2) 在N2保护下(或惰性气体),对硅烷气体进行检验。
SiH4+2KMnO4![]() H2+K2SiO3+2MnO2↓+
H2O (不要求)
H2+K2SiO3+2MnO2↓+
H2O (不要求)
(方程式各1分,检验1分)
略
(共8分) (1) 根据杂化轨道理论,下列离子或分子:NH3、NF3、NO2+中氮分别采用 、 、 杂化轨道同相应的键合原子成键。其中NH3的键角 (填“大于”或“小于”)NF3的键角的原因是 。
(2) 最近,德国科学家在医学杂志《柳叶刀》上发表文章,他们研究发现一种名为甘草甜素的物质可以有效抑制非典病毒的增殖,有望用其研制出治疗非典的特效药。此前医学家已用甘草甜素作为有效成分开发出药物,治疗丙肝与艾滋病等,并取得了一定效果。甘草甜素(甘草素)是甘草的根和茎中所含的一种五环三萜皂苷,其结构如图1所示:
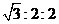
甘草甜素的(A)苷键构型为 ,将其水解可得到一分子的甘草次酸(如图2)和两分子的(填名称) ,其结构为:
。
知识点:分子结构与性质
(共8分) (1) sp3 sp3 sp
大于 氟的电负性大于氢,因此用于N-F成键的电子对更偏向氟 (或离氮原子核较远),氮周围电子密度减小(或N-F成键电子对间的“距离”较远),斥力较小,因而键角较小。
略
(共6分) 提出查理定律的查理很幸运,碰巧开始时没有以N2O4来研究气体行为,否则他或许会得出一种相当特殊的温度效应。
对于平衡N2O4(g)![]() 2NO2
(g),在 298K时其Kp=
0.1 pθ,而
2NO2
(g),在 298K时其Kp=
0.1 pθ,而![]() ,α为N2O4的离解度,p为平衡体系的总压。假设,298 K时,查理把0.015 mol的N2O4放于一只2.44×10
,α为N2O4的离解度,p为平衡体系的总压。假设,298 K时,查理把0.015 mol的N2O4放于一只2.44×10![]() m3的烧杯中,当离解达到平衡后,他将看到平衡压力等于0.205pθ。其对应的α = 0.33
m3的烧杯中,当离解达到平衡后,他将看到平衡压力等于0.205pθ。其对应的α = 0.33
(1) 在保持体积不变的前提下,查理做把温度升高10%的实验,即把温度升高至328K。根据理想气体定律,其压力也应只增大10%,即等于0.226pθ,但查理发现这时的压力为0.240pθ。自然,问题是出在N2O4的离解度增加上了。试求此时的α和Kp。
(2) 若NO2在298K下的标准摩尔生成自由能为51.463kJ·mol![]() ,试计算N2O4在298K下的标准摩尔生成自由能。
,试计算N2O4在298K下的标准摩尔生成自由能。
知识点:化学平衡状态及移动
(共6分)解:(1)在328K时,
![]()
= 0.02176(mol) 又n总 =
(1+α)n0 而n0
= 0.015 mol ∴![]()
则α = 0.451………………………………………(2分)
∴![]() ……(2分)
……(2分)
(2)
298K时,![]() 而
而![]()
∴![]() = − 8.314×298ln0.1=
5704.8(J·mol-1)
= − 8.314×298ln0.1=
5704.8(J·mol-1)
则![]() = 2×51.463×103 −
5704.8
= 2×51.463×103 −
5704.8
= 97.02(kJ·mol-1) …………………(2分)
略
(共6分) 世界各国科学家,从关注人类生存质量角度出发,将保护地球自然生态环境研究作为重大任务之一。并对与之相关的宇宙空间的复杂体系如太阳系进行了初步研究。结果发现太阳是一个巨大能源。它时刻都在向太空发射大量能量,其能量来源就是太阳时刻不停地进行着的链式聚变反应。在那里,氢原子核在极高温度下发生聚变反应。这种反应放出的能量,一方面用以维持反应必需的高温,另一方面则向太空辐射出能量。其中一种重要的聚变过程是碳一氮循环。这一循环是由一系列由碳-氮作媒介的反应组成的,并按下列步骤进行:
①
![]() ②
② ![]()
③
![]() ④
④ ![]()
⑤
![]() ⑥
⑥ ![]()
上述过程,放出的净能量为25.7MeV。每消耗1kg![]() H约产生6.2×1014J的能量。核聚变反应是太阳能够在几十亿年内稳定地发光释能的主要原因。
H约产生6.2×1014J的能量。核聚变反应是太阳能够在几十亿年内稳定地发光释能的主要原因。
(1) 在上述过程中x=
,y=
;x′=
,y′=
;![]() =
,
=
,![]() (均填数值)。
(均填数值)。
(2) 写出与净能量产生对应的反应方程式:
。
(3) 在反应中碳原子的作用是 。
知识点:原子结构与性质
(共6分)
(1) 13,6 14,7 15,7 ………………………(3分)
(2)
![]() …………(2分)
…………(2分)
(3) 催化剂 …………………………………………(1分)
略
(共7分) (1) 吸取KIO4和KIO3试液25.00mL,在弱碱性条件下加入过量Ⅺ溶液使IO4-还原成IO3-,并析出碘,用0.1000mol·L![]() 亚砷酸钠溶液滴定耗去10.00mL。
亚砷酸钠溶液滴定耗去10.00mL。
(2) 另取25.00mL该试液,在强酸性条件下,加入过量KI溶液,释放出的I2,用0.2000mol·L![]() Na2S2O3溶液滴定耗去50.00 mL。
Na2S2O3溶液滴定耗去50.00 mL。
写出有关的反应方程式:
每毫升试液中含KIO4 mg,KIO3 mg。
知识点:水的电离和溶液的酸碱性
(共7分)
(a) IO4-+2I-+H2O![]() IO3-+I2+2OH-
IO3-+I2+2OH-
(b)
AsO33-+I2+H2O![]() AsO43-+2I-+2H+
AsO43-+2I-+2H+
(c) IO4-+7I-+8H+![]() 4I2+4H2O
4I2+4H2O
(d) IO3-+5I-+6H+![]() 3I2+3H2O
3I2+3H2O
(e)
I2+2S2O32-![]() S4O6
S4O6![]() +2I-
+2I-
每毫升含KIO4 9.20 mg
KIO3 2.85 mg……………………(3分)
(反应式可以五个都写,也可以只写a、c、d或只写b、e(4分)
略

